Citidīns pieder nukleozīdiem un sastāv no nukleozās bāzes citozīna un cukura ribozes. Ar ūdeņraža saišu palīdzību tas veido bāzes pāri ar guanozīnu. Tam ir arī galvenā loma pirimidīna metabolismā.
Kas ir citidīns?
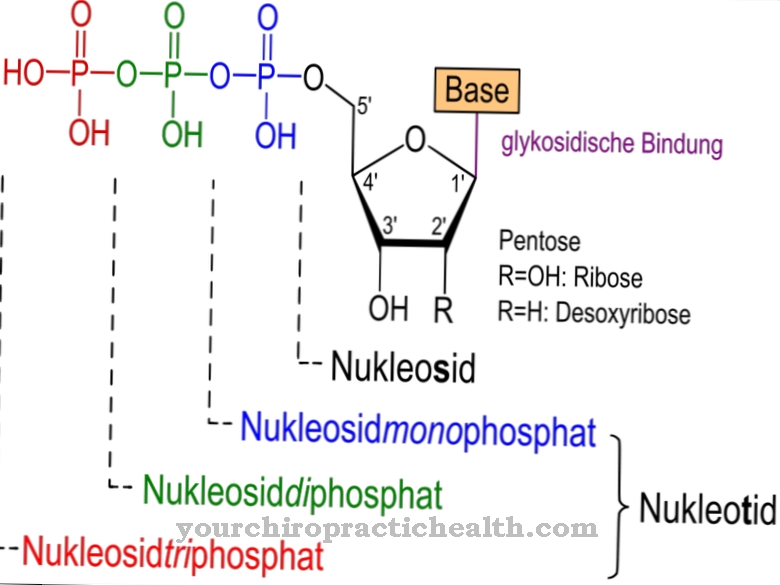
Citidīns ir nukleozīds, kas sastāv no citozīna un ribozes. Papildus adenīnam, guanīnam un timīnam nukleīnskābju sintēzē ir iesaistīts citozīna slāpekļa bāze. Citidīna fosforilēšana rada citidīna monofosfātu (CMP), citidīna difosfātu (CDP) vai citidīna trifosfātu (CTP).
Citidīna monofosfāts ir nukleotīds RNS. Nukleīnskābju struktūrā ir iesaistītas divas purīna un divas pirimidīna bāzes, ar timīnu RNS apmainoties pret uracilu. Adenīns un guanīns pieder pie purīna bāzēm, savukārt timīns, citozīns un uracils pieder pie pirimidīna bāzēm. Citidīna deamināze citamīnu var deaminēt par uridīnu. Uridīns ir nukleozīds, kas izgatavots no ribozes un uracila. To var arī fosforilēt par uridīna monofosfātu.
Uridīna monofosfāts ir arī svarīgs RNS nukleotīds. Turklāt CDP un CTP ir arī aktivējošās grupas lecitīna, cefalīna un kardiolipīna sintēzei. Tīrs citidīns ir ūdenī šķīstoša cieta viela, kas sadalās pie 201 līdz 220 grādiem. Ar enzīma pirimidīna nukleoidāzi to katalītiski var sadalīt līdz citozīnam un ribozei.
Funkcija, efekts un uzdevumi
Citidīnam ir galvenā loma pirimidīna metabolismā. Pirimidīns nodrošina nukleīnskābēs esošo citimīna, timīna un uracila pirimidīna bāzes struktūru. Tiamīns RNS tiek apmainīts pret uracilu.
Uracilu ražo arī, citamīnu deaminējot ar citidīna deamināzi. Ķīmiskajiem pārveidojumiem starp trim pirimidīna bāzēm ir galvenā nozīme atjaunošanas procesos DNS un epiģenētiskās izmaiņās. Epiģenētikas kontekstā dažādas īpašības mainās vides ietekmē. Tomēr ģenētiskais materiāls nemainās. Organisma modifikācijas izmaiņas izraisa atšķirīga gēnu ekspresija. Ķermeņa šūnu diferenciācijas procesi dažādu šūnu līniju un orgānu veidošanai atspoguļo arī epiģenētisko procesu.Atkarībā no šūnas veida tiek aktivizēti vai deaktivizēti dažādi gēni.
Tas notiek, metilējot citidīna bāzes DNS iekšienē. Metilēšanas laikā veidojas metilcitozīns, kuru deaminējot var pārveidot par timīnu. Komplementārs nukleāzes bāzes guanīns pretējā dubultā virknē ļauj atpazīt kļūdu un atkal timīnu apmainīt pret citozīnu. Tomēr guanīnu var arī apmainīt pret adenīnu, kas noved pie punktu mutācijas. Ja nemetilēts citozīns tiek deaminēts, tiek iegūts uracils. Tā kā uracils neparādās DNS, to nekavējoties aizstāj ar citozīnu. Citosīna vietā nedaudz palielina metilācijas izraisīto mutāciju ātrumu.
Tajā pašā laikā arvien vairāk un vairāk gēnu tiek izslēgti caur metilēšanu, lai šūnas šūnu līnijā kļūtu specializētākas. Remonta procesos remonta fermentu pamatā ir sākotnējā DNS virkne, kuru tie atpazīst ar augstāku metilācijas pakāpi. Papildu daļa ir veidota arī, pamatojoties uz tajā glabāto informāciju. Instalācijas kļūdas tiek nekavējoties izlabotas. Turklāt enzīma AID (aktivēšanas izraisīta citidīna dezamināze) ļoti specifiski katalizē citidīnu grupu atdalīšanu uridīna grupās vienpavediena DNS. Notiek somatiskas hipermutācijas, kas maina B šūnu antivielu secību. Tad tiek atlasītas atbilstošās B šūnas. Tas nodrošina elastīgu imūnreakciju.
Izglītība, sastopamība, īpašības un optimālās vērtības
Citidīns ir pirimidīna metabolisma starpprodukts. Kā izolētam savienojumam tas nav svarīgi. Kā jau minēts, tas sastāv no nukleīna bāzes citozīna un cidoniju cukura ribozes. Ķermenis pats var sintezēt citozīnu.
Tomēr tā sintēze ir ļoti energoietilpīga, tāpēc tā tiek reģenerēta no nukleīnskābju veidojošiem blokiem glābšanas ceļa ietvaros un to var atkārtoti integrēt nukleīnskābēs. Kad pamatne ir pilnībā sadalīta, rodas oglekļa dioksīds, ūdens un urīnviela. Tas atrodas RNS kā nukleozīds. DNS, citozīns ir saistīts ar dezoksiribozi, tā ka nukleozīdu dezoksicididīns šeit rodas kā celtniecības bloks.
Slimības un traucējumi
DNS citidīna atlikumu metilējumi ir ļoti svarīgi marķēšanai, lai atdalītu dažādus bioķīmiskos procesus. Tomēr kļūdas var rasties arī metilēšanā, kas noved pie slimības.
Bojātu metilējumu gadījumā var izraisīt gan palielinātu, gan samazinātu gēnu aktivitāti, kas neatbilst prasībām. Šīs metilēšanas shēmas tiek nodotas šūnu dalīšanas laikā. Ilgtermiņā notiek izmaiņas, kas var izraisīt slimības. Piemēram, dažām audzēja šūnām ir dažādas metilācijas struktūras, kas nenotiek veselās šūnās. Piemēram, metilēšana var bloķēt noteiktus gēnus, kas kodē augšanu regulējošos enzīmus. Ja šo enzīmu trūkst, var notikt neattīstīta šūnu augšana. Tas attiecas arī uz fermentiem, kas, sākoties šūnu defektiem, sāk organizētu šūnu nāvi (apoptozi).
Mērķtiecīga DNS metilēšanas ietekmēšana vēl nav iespējama. Tomēr ir pētījumi par pilnīgu audzēja šūnu demetilēšanu, lai tās atkal pakļautu augšanu regulējošo olbaltumvielu kontrolei. Saskaņā ar vairākiem klīniskiem pētījumiem ir pierādīts, ka demetilēšana ierobežo audzēja augšanu pacientiem ar akūtu mieloleikozi. Šo procedūru sauc arī par epiģenētisko terapiju. Metilācijas procesiem var būt nozīme arī citās slimībās. Vides ietekmes dēļ organisms pielāgojas mainīgiem apstākļiem, veidojot bioloģiskas modifikācijas, kuru pamatā ir DNS citidīna atlikumu metilēšana. Tādējādi ķermenis veic mācību procesu, kas tomēr var izraisīt arī nepareizu regulēšanu.




.jpg)




.jpg)