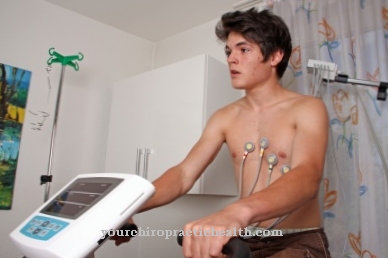
Adenozīna monofosfāts ir nukleotīds, kas var būt daļa no enerģijas nesēja adenozīna trifosfāta (ATP). Kā ciklisks adenozīna monofosfāts tas darbojas arī kā otrais kurjers. Tas, cita starpā, tiek izveidots, sadaloties ATP, kas atbrīvo enerģiju.
Kas ir adenozīna monofosfāts?
Adenozīna monofosfāts (C10H14N5O7P) ir nukleotīds un pieder pie purīna ribotīdiem. Purīns ir celtniecības materiāls cilvēka ķermenī, kas atrodams arī visās citās dzīvajās lietās. Molekulā veidojas divkāršs gredzens un tā nekad neparādās viena pati: purīns vienmēr ir saistīts ar citām molekulām, veidojot lielākas vienības.
Purīns ir viens no adenīna celtniecības blokiem. Šī bāze ir atrodama arī dezoksiribonukleīnskābē (DNS) un kodē ģenētiski glabātu informāciju. Papildus adenīnam purīna bāzēm pieder arī guanīns. Adenozīna monofosfātā esošais adenīns ir saistīts ar diviem citiem celtniecības blokiem: ribozi un fosforskābi. Ribose ir cukurs ar molekulāro formulu C5H10O5. Bioloģija molekulu sauc arī par pentozi, jo tā sastāv no piecu locekļu gredzena. Adenozīna monofosfātā fosforskābe saistās ar piekto ribozes oglekļa atomu. Citi adenozīna monofosfāta nosaukumi ir adenilāts un adenilskābe.
Funkcija, efekts un uzdevumi
Cikliskais adenozīna monofosfāts (cAMP) atbalsta hormonālo signālu pārraidi. Piemēram, steroīdais hormons saistās ar receptoru, kas atrodas ārpus šūnas membrānas. Savā ziņā receptors ir šūnas pirmais saņēmējs. Hormons un receptors sader kopā kā atslēga un slēdzene, tādējādi šūnā izraisot bioķīmisku reakciju.
Šajā gadījumā hormons ir pirmais kurjers, kas aktivizē enzīma adenilāta ciklāzi. Šis biokatalizators tagad sadala ATP šūnā, izveidojot cAMP. Tad cAMP savukārt aktivizē citu enzīmu, kas atkarībā no šūnas veida izraisa šūnas reakciju - piemēram, jauna hormona ražošanu. Adenozīna monofosfāts ir jūsu otrās signālvielas vai otrā kurjera funkcija.
Tomēr molekulu skaits nepaliek vienāds katrā solī: Molekulu skaits vienā reakcijas solī palielinās apmēram desmit reizes, kas palielina šūnas reakciju. Tas ir arī iemesls, kāpēc hormoni ir pietiekami ļoti zemā koncentrācijā, lai izraisītu spēcīgu reakciju. Reakcijas beigās viss, kas paliek no cAMP, ir adenozīna monofosfāts, kuru citi fermenti var atgriezties ciklā.
Kad ferments sadala AMP no adenozīna trifosfāta (ATP), rodas enerģija. Cilvēka ķermenis dažādi izmanto šo enerģiju. ATP ir vissvarīgākais enerģijas nesējs dzīvās būtnēs un nodrošina, ka bioķīmiskie procesi var notikt mikro līmenī, kā arī muskuļu kustības.
Adenozīna monofosfāts ir arī viens no ribonukleīnskābes (RNS) celtniecības blokiem. Cilvēka šūnu kodolā ģenētiskā informācija tiek glabāta DNS formā. Lai šūna varētu ar to strādāt, tā kopē DNS un izveido RNS. DNS un RNS satur vienādu informāciju par vienu un to pašu sadaļu, taču atšķiras pēc to molekulu struktūras.
Izglītība, sastopamība, īpašības un optimālās vērtības
Adenozīna monofosfāts var rasties no adenozīna trifosfāta (ATP). Fermenta adenilāta ciklāze sašķeļ ATP un procesa laikā atbrīvo enerģiju. Īpaši nozīmīgu lomu spēlē vielu fosforskābe. Fosfoanhidrīta saites saista atsevišķās molekulas viena ar otru. Šķelšanai var būt vairāki iespējamie iznākumi: vai nu fermenti sadala ATP adenozīndifosfātā (ADP) un ortofosfātā, vai arī AMP un pirofosfātā. Tā kā enerģijas metabolisms būtībā ir cikls, fermenti var arī apvienot atsevišķos veidojošos blokus atpakaļ ATP.
Mitohondriji ir atbildīgi par ATP sintēzi. Mitohondriji ir šūnu organellās, kas darbojas kā šūnu spēkstacijas. No pārējās šūnas tos atdala ar pašu membrānu. Mitohondriji tiek mantoti no mātes (mātes). Adenozīna monofosfāts notiek visās šūnās, tāpēc to var atrast visur cilvēka ķermenī.
Slimības un traucējumi
Ar adenozīna monofosfātu var rasties vairākas problēmas. Piemēram, var tikt traucēta ATP sintēze mitohondrijos. Arī medicīna šādu disfunkciju sauc par mitohondriju slimību. Tam var būt dažādi cēloņi, ieskaitot stresu, sliktu uzturu, saindēšanos, brīvo radikāļu bojājumus, hronisku iekaisumu, infekciju un zarnu slimības.
Ģenētiski defekti bieži ir atbildīgi par sindroma attīstību. Mutācijas maina ģenētisko kodu un izraisa dažādus traucējumus enerģijas metabolismā vai molekulu struktūrā. Šīs mutācijas nav obligāti atrodamas šūnas kodola DNS; Mitohondrijiem ir savs ģenētiskais sastāvs, kas pastāv neatkarīgi no šūnas kodola DNS.
Mitohondriopātijā mitohondriji ATP ražo tikai lēnāk; tāpēc šūnām ir mazāk enerģijas. Tā vietā, lai izveidotu pilnīgu ATP, mitohondriji sintezē vairāk ADP nekā parasti. Šūnas var arī izmantot ADP enerģijas ražošanai, bet ADP izstaro mazāk enerģijas nekā ATP. Mitohondriju slimības gadījumā organisms var izmantot glikozi kā enerģijas piegādātāju; kad tie tiek sadalīti, tiek ražota pienskābe. Mitohondriju slimība pati par sevi nav slimība, bet ir sindroms, kas var būt daļa no slimības.
Medicīna apkopo dažādas mitohondriju traucējumu izpausmes zem nosaukuma. Tas var rasties, piemēram, MELAS sindroma kontekstā. Šī ir neiroloģiska slimība, kurai raksturīgi krampji, smadzeņu bojājumi un pastiprināta pienskābes veidošanās. Turklāt mitohondriju slimība ir saistīta arī ar dažādām demences formām.

.jpg)
.jpg)



.jpg)
.jpg)