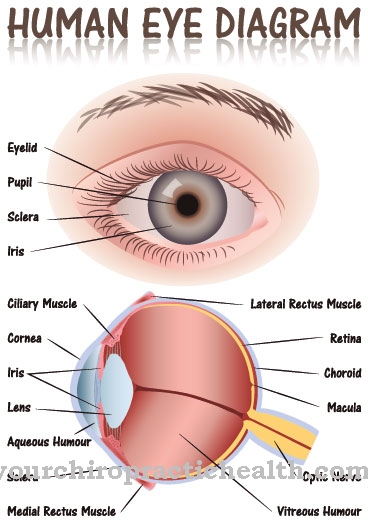
Kalcineurīns (CaN) ir olbaltumvielu fosfatāze, kurai ir nozīmīga loma imūnsistēmas T šūnu aktivizēšanā, bet tā ir aktīva arī citos organismā ar kalciju saistītos signalizācijas ceļos. Defosforilējot NF-AT olbaltumvielu, šis ferments sāk virkni gēnu transkripciju, kas galvenokārt ir atbildīgas par T limfocītu raksturīgo darbu. Pateicoties šai galvenajai pozīcijai, kalcineirīns ir sākumpunkts vairākām imūnsupresijas terapeitiskajām metodēm.
Kas ir kalcineurīns?
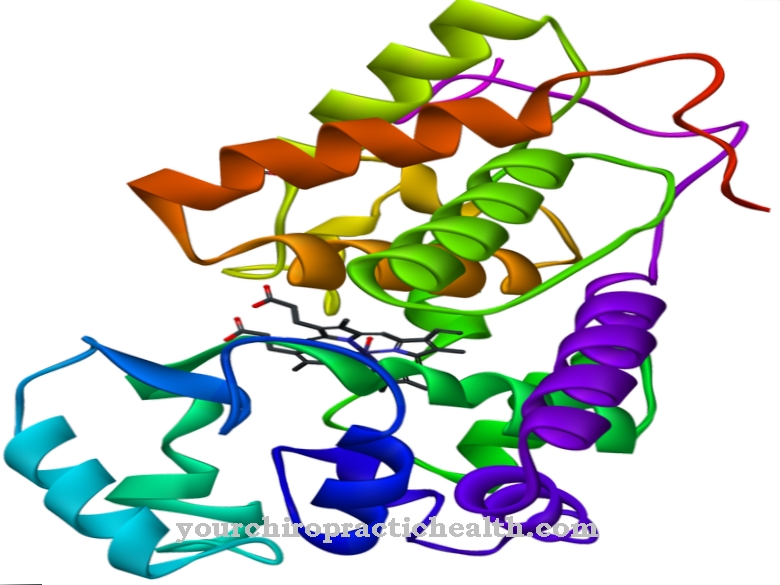
Fermentu veido divas apakšvienības: Kalcineurīns A (aptuveni 60 kDa) rūpējas par katalītisko funkciju un tam ir kalmodulīna saistīšanās vieta, savukārt kalcineurīns B (aptuveni 19 kDa) ir normatīvi aktīvs un tam ir divas kalcija jonu saistīšanas vietas.
Savā pamata stāvoklī CaN ir neaktīvs, jo daļa olbaltumvielu bloķē aktīvo centru - to sauc par autoinhibīciju. Pilnīgai aktivizēšanai nepieciešama kalcija aktivēta kalmodulīna un kalcija jonu saistīšana. Kalcineurīnam kā fosfatāzei tiek piešķirts EK numurs 3.1.3.16, kas satur tos enzīmus, kas katalizē serīna un citu olbaltumvielu treonīna atlikumu hidrolītisko defosforilēšanu.
Funkcija, efekts un uzdevumi
Īpaši selektīva ir fermenta saistīšanas vieta substrātā NF-ATc (aktivēto T-šūnu kodolu faktors, citosola). Šis transkripcijas faktors ir atrodams limfocītu šūnu plazmā. Zemes stāvoklī NF-Atc ir fosforilēts un tāpēc neaktīvs.
Kalcineurīna loma imūnā atbildē sākas ar antigēna uzņemšanu - piemēram, vīrusa, baktērijas vai deģenerētu šūnu komponentus - imūnās sistēmas šūnās (monocīti, makrofāgi, dendrītiskās šūnas un B šūnas). Pēc tam šo vielu apstrādā un uzrāda uz šūnas virsmas.
Kad antigēnus prezentējošās šūnas nonāk saskarē ar T-šūnu T-šūnu receptoru, tiek aktivizēta signāla kaskāde. Šie ārpusšūnu stimuli palielina kalcija koncentrāciju šūnā. Kalcija joni saistās ar CaN B, kas, mainot olbaltumvielu struktūru, izšķīdina CaN A autoinhibitoru domēnu un pastarpināti nodrošina kalodulīna saistīšanos ar CaN A. Tas padara kalcineirīnu pilnīgi katalītiski aktīvu un defosforilē ar serīniem bagāto reģionu (SRR) NF-ATc aminoterminālajā stāvoklī. Tā rezultātā mainās NF-ATc konformācijas izmaiņas, kā rezultātā transkripcijas faktors tiek transportēts šūnas kodolā. Tur tas izraisa vairāku gēnu, kas cita starpā ir atbildīgi par interleikīnu, piemēram, IL-2, ražošanu, transkripciju.
IL-2 nodrošina arī T palīgu šūnu aktivizēšanu un citokīnu sintēzi, tādējādi vadot citotoksisko T šūnu darbu. Kamēr palīgu šūnas kontrolē citus imūnās atbildes limfocītus - piemēram, nobriedinot B šūnas plazmas šūnām vai atmiņas šūnām un aktivizējot fagocītus - citotoksiskās T šūnas ir atbildīgas par inficēto vai deģenerēto šūnu iznīcināšanu organismā. Tā kā šo ceļu nevar iziet bez kalcineirīna, imūnsistēmas reakcijā galvenā loma ir fermentam.
Turpmākie enzīma mērķa proteīni ir cAMP atbildes elementu saistošais proteīns (CREB) ar ietekmi, piemēram, uz nervu sistēmu un iekšējo pulksteni un miocītu pastiprinošo faktoru 2 (MEF2), kas daļēji ir atbildīgs par šūnu diferenciāciju embriju attīstībā un spēlē lomu dažu audu reakcijā uz stresu pieaugušajiem.
Izglītība, sastopamība, īpašības un optimālās vērtības
Abu subvienību izoformas ir atšķirīgas (CaN A: 3 izoformas, CaN B: 2 izoformas), dažas no tām ir izteiktas atšķirīgi atkarībā no ķermeņa reģiona. Jo īpaši izceļas CaN A γ, kas rodas tikai sēkliniekos un ir iesaistīts tur sēklu nogatavināšanā. Neskatoties uz nozīmīgo lomu, kāda tai ir imūnsistēmā un nervos, var pieņemt, ka kalcineurīns ir atrodams gandrīz visos audos. Regulēšana notiek mazāk, palielinot vai samazinot sintēzi, bet gan caur kalcineurīna inhibitoru CAIN. Tas novērš, piemēram, NF-AT defosforilēšana.
RCAN1 negatīvā atgriezeniskās saites regula nodrošina, ka nerodas pārāk augsta CaN citosola koncentrācija. Aktivizēts (defosforilēts) NF-AT saistās ar RCAN1 gēna veicinātāju šūnas kodolā un tādējādi izraisa transkripciju. Iegūtais RCAN1 saistās ar CaN un kavē tā darbību.
Slimības un traucējumi
Kalcineurīns ir tādu kalcineurīna inhibitoru mērķis kā Ciklosporīns, pimekrolīms un takrolīms. Inhibējot CaN fosfatāzes darbību, tiek izraisīta imūnsupresija, kas, piem. pēc orgānu transplantācijas, lai samazinātu atgrūšanas iespējamību, vai autoimūno slimību gadījumā, lai apkarotu iekaisuma procesus.
Tādējādi CaN inhibitorus izmanto arī slimību ārstēšanai no reimatoīdās grupas. Citas pašlaik pētītās pieejas ir cīņa pret tuberkulozi, šizofrēniju un diabētu. CaN A γ ekskluzīvā klātbūtne sēkliniekos norāda uz iespējamu lomu kontracepcijas līdzekļu attīstībā. Sirds hipertrofijas gadījumos, kad ir iesaistīts CaN-NA-FT signāla ceļš, hipertrofijas attīstību var novērst, ievadot CaN inhibitorus.
Cilvēkiem ar Dauna sindromu parasto divu vietā ir trīs 21 hromosoma, kas kodē kalcineirīnu kavējošu olbaltumvielu. Šis inhibitors neļauj kalcineurīnam mijiedarboties ar asinsvadu šūnām un izraisīt proliferācijas procesus tajās. Šis fakts ir īpaši svarīgs audzēju gadījumā, jo tie, cita starpā, nodrošina asins piegādi caur kalcineirīnu. Iejaukšanās šajā brīdī var efektīvi novērst vēža progresēšanu. Tātad jūs varat atrast piem. ievērojami zemāks audzēju biežums cilvēkiem ar Dauna sindromu un cer, ka mērķtiecīga šī procesa kavēšana nākotnē sniegs priekšrocības cīņā pret vēzi.
Nesen arvien vairāk pierādījumu ir arī tam, ka ar vecumu saistīta kalcineurīna disregulācija varētu būt nozīmīga arī tādu neironu slimību kā Alcheimera slimība attīstībā. Signalizācijas ceļu, kuros ferments ir iesaistīts, pētījumi atklāj arvien vairāk balto plankumu bioķīmiskajā kartē. Tajā pašā laikā tas paver cerību, ka ar šī galvenā proteīna palīdzību mēs nākotnē spēsim labāk izprast un ārstēt lielu skaitu dažādu slimību.



.jpg)






.jpg)